
 |
|---|
| Accueil | Le fonctionnement | Usages et Dangers | Limites législatives et éthiques | Conclusion |
|---|---|---|---|---|
| Bibliographie | Remerciements | Sondage | Protocole expérimental | Lexique |
|
LA TECHNIQUE DU CLONAGE THERAPEUTIQUE a. L’apparition de la technique En 1998, ce sont les américains James Thomson, Joseph Istkovitz-Eldor et l'israélien Benjamin Reubinoff qui ont découvert des cellules pluripotentes dans des embryons humains au stade de blastocyste (environ entre 5 et 7 jours de développement). Ces cellules, dites cellules ES (embryonnaires souches) ne sont pas différenciées et servent à former tous types de tissus de l'organisme. De plus, elles se multiplient facilement dans un milieu de culture adéquat. Cette découverte a permit douvrir la perspective de clonage thérapeutique. 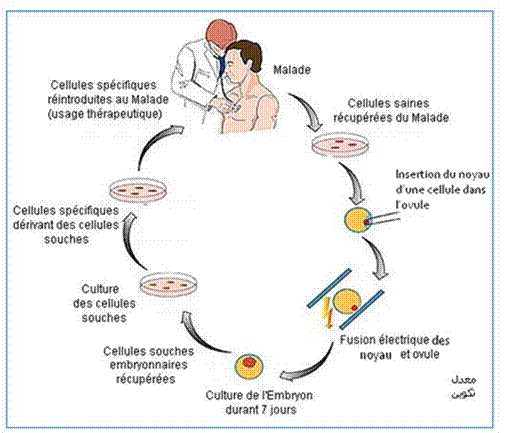
Déroulement d’un clonage thérapeutique par transfert de noyau Le premier et plus ancien principe du clonage thérapeutique consiste à créer, en transférant le noyau d’une cellule du patient dans un ovocyte énuclée, un embryon afin d'en prélever les cellules ES. Elles sont alors différenciées de façon dirigée. Il n'y a plus alors qu'à remplacer les cellules défaillantes du malade par celles formées à partir des cellules ES, sans risque de rejet puisque les cellules auront été prélevées sur le « clone » du patient.
d. La différenciation des cellules ES Les cellules de l’embryon cloné possèdent la même information génétique que les cellules du donneur. On arrête son développement lorsqu’il est devenu un blastocyste, pour récupérer les cellules ES. Cependant, comme il est interdit de cloner des embryons humains, on utilise des embryons de souris clonées et des embryons surnuméraires pour les recherches sur les cellules ES.
Les cellules ES sont prélevées dans
la masse cellulaire interne du blastocyste. De ce fait, elles ne peuvent pas
devenir un organisme complet, alors que le placenta nourrissant l'embryon et
le protégeant de tout rejet immunitaire est formé par le trophectoderme*.
Les cellules ES obtenues sont ensuite mises en culture, car elles sont immortelles
(elles ont la faculté de se reproduire à l'infini comme les cellules
cancéreuses). En cultivant les cellules ES dans des milieux de cultures
adéquats, on peut obtenir ainsi des lignées de cellules souches
embryonnaires, qui sont conservées dans des boîtes de pétri.
En novembre 2007, des chercheurs de l'Institut André Lwoff, en partenariat
avec le CNRS, ont obtenu la première lignée française
de cellules souches embryonnaires humaines. d. Les limites de la technique du transfert de noyau Tout d'abord, les essais chez les animaux ne sont pas concluants. En effets, seule une très faible proportion des clonages expérimentaux effectués sur des animaux ont pu être menés à terme. Selon les méthodes employées et les espèces, près de deux tiers des embryons clonés par transfert de noyau aboutissent, mais seulement un à quatre pour cent des embryons se développent à terme. A cela on peut ajouter que le taux est nul pour les primates.
Etude statistique du nombre de clonages par transfert de noyau menée à terme entre 2002 et 2007 D'autre part, produire des tissus par clonage thérapeutique nécessite de mettre en culture des cellules embryonnaires, puis de leur donner un signal pour les pousser à se différencier. Or, la technique de différenciation est complexe et loin d'être maîtrisée. Finalement, et certainement le plus problématique, la moindre erreur lors de la différenciation des cellules ES pourrait provoquer une tumeur, car, comme nous l’avons dis plus tôt, il y a une forte ressemblance entre les cellules cancéreuses et les cellules souches embryonnaires.
I. Les cellules IPS (induced pluripotent stem cells) a. L’apparition de la technique et son principe Des scientifiques ont étudié ce qui
distinguait les cellules souches embryonnaires des autres cellules. Après
de nombreuses études Ils ont constaté qu'une vingtaine de gènes
s'activaient ensemble durant les premiers jours de l'embryon, et s‘éteignaient
ensuite au moment de leur spécialisation. Pour en savoir plus, des chercheurs
japonais ont sélectionné quatre de ces gènes qui paraissaient
jouer un rôle important, qu'ils ont ensuite inséré dans
une cellule de souris. Après observation, ces gènes implantés
ont déclenché l'activité des autres gènes qui ont
engendré la reprogrammation des cellules. Ces cellules sont qualifiées
d’IPS puisqu'elles peuvent devenir n’importe quel type de cellule
d'une souris alors qu’elles avaient déjà été différenciées.
Après un an de recherches deux laboratoires, un Américain et
l’autre Japonais ont montré que cette méthode fonctionnait
aussi sur les cellules humaines.
Déroulement d’un clonage thérapeutique à l’aide des cellules IPS b. Les limites de la technique d’utilisation des cellules IPS Malgré les attraits positifs
de cette technique de clonage, il y a aussi de nombreux inconvénients.
En premier lieu, 20% des cellules réimplantées deviennent un
cancer. Même si, de nos jours, les scientifiques ont les moyens de détruire
le cancer dès sa formation, le clonage aurait néanmoins été inutile
puisque les cellules auraient été détruites avec le cancer.
De plus, même si les cellules IPS ressemblent beaucoup aux cellules ES,
il reste tout de même près de mille gènes qui ne sont pas
exprimées dans les cellules IPS qui le sont dans les cellules ES. Malgré les nombreuses limites qui empêchent l’épanouissement
total du clonage thérapeutique on y trouve
|
|---|